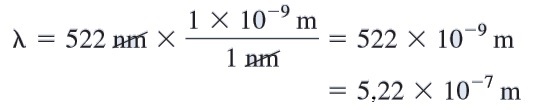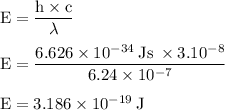Latihan dan Kuis (1)
a) latihan 1
1. example 7.1
Panjang gelombang lampu hijau dari sinyal lalu lintas dipusatkan pada 522 nm. Berapa frekuensi radiasi ini?
Strategi
Diketahui panjang gelombang dari gelombang elektromagnetik dan diminta untuk menghitung frekuensinya. Menyusun ulang Persamaan (7.1) dan mengganti 𝛖 dengan c (kecepatan cahaya) memberikan
𝛖 = c / 𝛌
Penyelesian
Karena kecepatan cahaya diberikan dalam meter per detik,pertama akan lebih mudah untuk mengkonversi panjang gelombang menjadi satuan meter. Ingat bahwa 1 nm = 1 x 10⁻⁹ m
Kita dapat menuliskan
Strategi
Penyelesaian
Dari Persamaan (7.6) kami menulis
Kita dapat mengganti panjang gelombang 5,22 x 10⁻⁷ m dan kecepatan cahaya 3,00 x 10⁸ m/s, sehingga frekuensinya adalah
2. example 7.2
Hitung energi (dalam joule) dari (a) foton dengan panjang gelombang 5,00 x 10⁴ nm (wilayah inframerah) dan (b) foton dengan panjang gelombang 5,00 x 10⁻² nm (wilayah sinar X).
Strategi
Baik dalam (a) dan (b) kita diberi panjang gelombang foton dan diminta untuk menghitung energinya. Kita perlu menggunakan Persamaan (7.3) untuk menghitung energi. Konstanta Planck diberikan dalam lampiran.
Penyelesaian
Dari persamaan 7.3
Ini adalah energi dari satu foton dengan panjang gelombang 5,00 x 10⁴ nm.
(b) Dengan mengikuti prosedur yang sama seperti pada (a), kita dapat menunjukkan bahwa energi foton yang memiliki panjang gelombang 5,00 x 10⁻² nm adalah 3,98 x 10⁻¹⁵ J.
3. example 7.4
Berapa panjang gelombang foton (dalam nanometer) yang dipancarkan selama transisi dari keadaan ni = 5 ke keadaan nf = 2 dalam atom hidrogen?
Strategi
Diketahui status awal dan akhir dalam proses emisi. Kita dapat menghitung energi foton yang dipancarkan menggunakan Persamaan (7.6). Kemudian dari Persamaan (7.2) dan (7.1) kita dapat menyelesaikan untuk panjang gelombang foton. Nilai konstanta Rydberg diberikan dalam teks.
Penyelesaian
Dari Persamaan (7.6) kami menulis
Tanda negatif menunjukkan bahwa ini adalah energi yang terkait dengan proses emisi. Untuk menghitung panjang gelombang, kita akan menghilangkan tanda minus untuk 𝚫E karena panjang gelombang foton harus positif. Karena 𝚫E = h𝛎 atau 𝛎 = 𝚫E/h, kita dapat menghitung panjang gelombang foton dengan menulis
b) kuis 1
1. Problem 7.15
Foton memiliki panjang gelombang 624 nm. Hitung energi foton dalam joule.
Diberikan :